近日,医学影像学院微流控技术与先进材料科研团队在《ACS Sensors》(中科院一区,Top期刊,影响因子8.3)上发表了题为“Ultrasensitive Detection of Extracellular Vesicles Based on Metal-Organic Framework DNA Biobarcodes Triggered G-quadruplex Coupled with Rolling Circle Amplification Assay”的研究论文。医学影像学院医学工程学教研室高彦峰为论文的共同通讯作者,皖南医学院为文章的共同通讯单位。
细胞外囊泡(EVs)是肿瘤细胞分泌的纳米级颗粒,携带蛋白质、核酸等特异性生物标志物,被视为癌症“液体活检”的重要靶标。然而,EVs体积小(50-200 nm)、丰度低且成分复杂,传统检测技术存在灵敏度不足、操作繁琐等局限。针对这一难题,研究团队提出了一种基于锆基金属有机框架(Zr-MOF)与级联信号放大的创新策略。具体而言,研究团队通过Zr-MOF纳米颗粒表面修饰的抗体特异性捕获EVs,并通过磷酸盐触发Zr-MOF的降解释放DNA条形码,将EVs的数量转化为可扩增的核酸信号。随后,释放的DNA条形码激活滚环扩增(RCA)反应,生成重复长链DNA并组装形成G-四链体结构。结合血红素后,这些G-四链体作为类酶催化单元,显著放大检测信号(图1)。该平台支持高灵敏度荧光检测与可视化比色分析,结果可交叉验证,适用于实验室精准检测与基层医疗现场快速筛查。该平台在卵巢癌临床样本的检测中表现优异,对EpCAM、CD24等肿瘤标志物的检测灵敏度高达97%以上,能够在5小时内准确区分患者与健康人群,检测限低至每毫升100个EVs。相比传统的超速离心和微流控方法,这一策略无需复杂设备,成本更低,便于在资源有限的医疗环境中推广应用。
这项研究的成功为肿瘤无创诊断开辟了新路径,具有良好的临床转化潜力,将推动液体活检在肿瘤早期筛查中的普及和应用,为实现肿瘤早发现、早干预提供了有效手段。(高彦峰 /文、图)
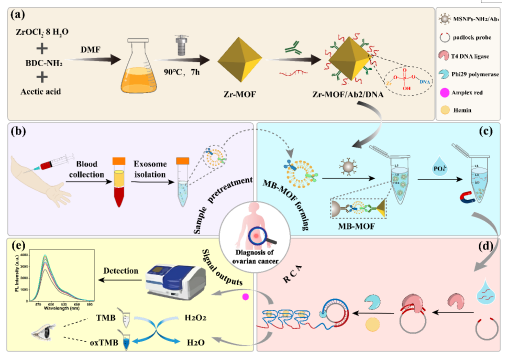
图1. 基于MOF-DNA生物条形码与G-四链体/滚环扩增系统的细胞外囊泡检测原理图
原文链接:https://doi.org/10.1021/acssensors.4c03384